“¿Hasta dónde seguir persiguiendo un parásito, un insecto, una enfermedad que como un fantasma que no se alcanza nunca, parece estar siempre más allá?”, se pregunta Salvador Massa en Casas de fuego (1995), la película que retrata la lucha del médico argentino contra la enfermedad descubierta por Carlos Chagas en 1909.
Pasan los años, y el parásito Trypanosoma cruzi sigue generando uno de los problemas de salud pública más relevantes de América Latina, especialmente entre sectores vulnerables. Desde 2009, cada 14 de abril, una efeméride recuerda el primer diagnóstico realizado por el médico brasileño al identificar las causas de esta infección.
Conscientes de la gravedad de esta problemática, desde hace décadas, equipos científicos de la Facultad de Ciencias Químicas (UNC) abordan el estudio de la enfermedad de Chagas desde diferentes perspectivas. La mayoría de los grupos surgieron tras la finalización de los postdoctorados de sus directoras en el exterior.
Cada línea tiene un enfoque específico que abarca desde el estudio de la vinchuca, el vector que transmite el parásito que causa la enfermedad, hasta los efectos de la infección en el sistema inmunológico de las personas y los tratamientos para enfrentarla.
Desde el 2000, un equipo liderado por Lilián Canavoso aborda el estudio bioquímico de la reproducción de las vinchucas, con énfasis en el impacto del estado nutricional sobre la ovogénesis (formación de huevos) y el desarrollo del tejido ovárico de estos insectos. El grupo también estudia proteínas vegetales (ureasas) y moléculas derivadas para el control de vinchucas como alternativas al uso de insecticidas químicos.

Por su parte, desde 2001, Pilar Aoki se centra en el estudio de los mecanismos inmunológicos que activa el tejido cardíaco frente al Trypanosoma cruzi, tanto en modelos experimentales como en la patología humana. En los últimos años, la científica y su equipo también han comenzado a explorar la optimización del tratamiento de esta enfermedad, obteniendo resultados pioneros a nivel internacional.
Desde 2008, Eva Acosta viene consolidando una línea que integra modelos experimentales y estudios traslacionales. El trabajo de su equipo se centra en el efecto inflamatorio que ocurre en las personas. Su grupo también se enfoca en el rol de las células T regulatorias (Tregs), una subpoblación del sistema inmune encargada de modular la respuesta antiparasitaria y contribuir a limitar el daño tisular (lesión o destrucción de tejidos) que genera la infección.
Estos grupos científicos se desempeñan en diferentes laboratorios con sede en el Departamento de Bioquímica Clínica y el Centro de Investigaciones en Bioquímica Clínica e Inmunología (CIBICI), de la FCQ (UNC)-CONICET.
Con foco en las vinchucas
“Nuestra investigación busca identificar procesos biológicos clave -como la señalización hormonal- que puedan derivar en el desarrollo de herramientas biotecnológicas más precisas. En particular, el estudio de toxinas entomológicas de origen vegetal como la ureasa Jack Bean Urease (JBU), una proteína con potencial insecticida que resulta segura para la humanidad y el ambiente, aporta información para avanzar hacia estrategias de control de estos insectos más selectivas”, señaló Canavoso.
Al estudiar las vinchucas, su equipo combina enfoques bioquímicos, fisiológicos, celulares y moleculares destinados a conocer los efectos entomotóxicos que las ureasas tienen sobre los sistemas reproductivo e inmune de estos insectos hematófagos. Las ureasas son capaces de generar toxicidad y su muerte, por lo que resultan agentes de control biológico al dañar sus tejidos internos, inhibir su alimentación o alterar su metabolismo.
Junto a colegas y estudiantes de Bioquímica y de la Licenciatura en Biotecnología, la científica estudia la fisiología de algunas especies de vinchucas, enfocándose en sus procesos de defensa e inmunidad y en su reproducción, con el objetivo de contribuir al desarrollo de estrategias de control vectorial más racionales y ambientalmente seguras.

Este grupo logró aportes a desafíos sanitarios internacionales. Entre ellos, avanzó en la comprensión del proceso reproductivo de la especie Dipetalogaster maxima, al identificar el rol de la hormona juvenil y de su receptor Met en la producción de huevos, y en la caracterización de las células responsables de la respuesta inmune llamadas hemocitos.
Asimismo, estudió el efecto de la ureasa vegetal JBU. El desarrollo de alternativas para combatir a las vinchucas de forma más específica y sustentable es uno de sus grandes potenciales. Por estos días, investiga a la especie Rhodnius prolixus, de gran relevancia epidemiológica. “Estamos analizando cómo la JBU interfiere en su reproducción y activa sus respuestas inmunes”, dijo Canavoso.

Para estudiar estos insectos, resulta clave disponer de equipos de trabajo y espacios especializados como insectarios y centros de referencia. En ese sentido, la científica manifestó su preocupación por la falta de acceso a recursos biológicos estratégicos en el futuro ante el cierre de instituciones como la unidad operativa de Santa María de Punilla, un referente a nivel nacional en vectores de Chagas.
“La interrupción de estos procesos no solo impacta en la investigación básica, sino que limita el desarrollo de herramientas para el control vectorial de la enfermedad, que continúa afectando a poblaciones vulnerables”, expresó la especialista, quien trabaja en esta línea desde los años ´90.
La protección del corazón desde la inmunología
Pilar Aoki es bioquímica y farmacéutica. Actualmente, se desempeña como directora del Departamento de Bioquímica Clínica y vicepresidenta de la Sociedad Argentina de Inmunología. En la FCQ, dirige 2 líneas de estudio sobre la enfermedad de Chagas.
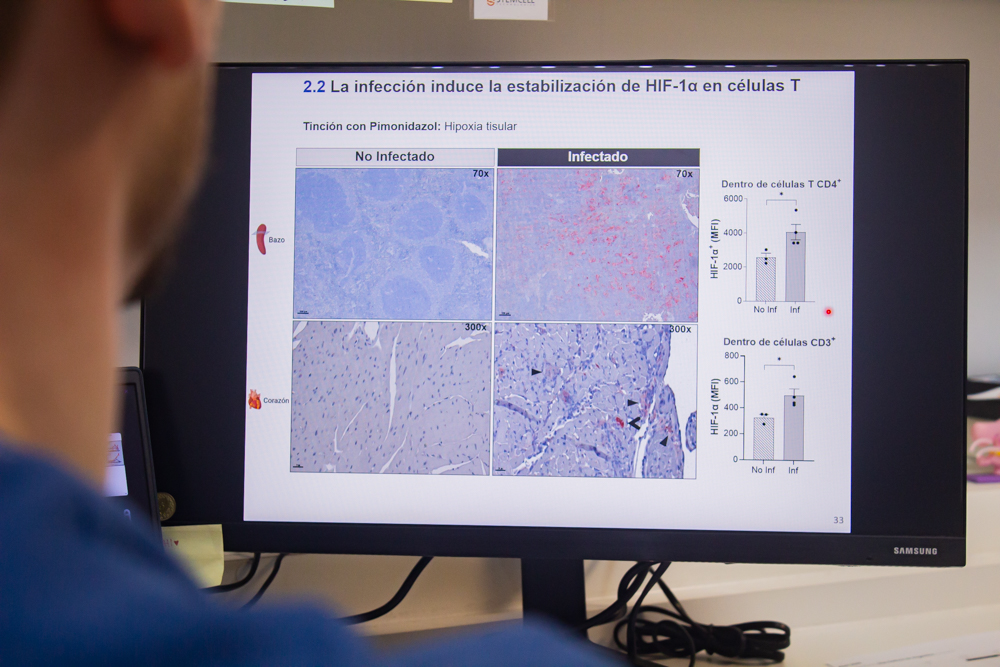
Por un lado, investiga la respuesta inmune del tejido cardíaco ante una infección, empleando como modelo el parásito Trypanosoma cruzi, que presenta un tropismo especial por el corazón. Amplía los alcances de este estudio investigando cómo se dan estos mecanismos en pacientes con diabetes tipo 2. Por otro lado, Aoki y su equipo exploran la optimización del tratamiento de la enfermedad de Chagas.

En este tiempo, el grupo alcanzó resultados inéditos de trascendencia internacional. “Históricamente, el tejido cardíaco era considerado un bystander, una especie de “testigo pasivo” de los procesos infecciosos y metabólicos. Nuestro equipo fue pionero en establecer la participación del sistema purinérgico en el control de la respuesta inmune que se da en ese «campo de batalla»”, explicó la inmunóloga.
El sistema purinérgico es un mecanismo de señalización celular en el que moléculas que componen los ácidos nucleicos llamadas nucleótidos, como ATP y ADP, y otros nucleósidos, como adenosina, actúan como señalizadores en la neurotransmisión, la respuesta inmune y la inflamación, entre otros procesos fisiológicos.
“Una vez que el parásito ingresa al tejido cardíaco, numerosas células inmunes acuden al sitio para detener la infección. Esto provoca una disminución del oxígeno, lo que hace que las células del miocardio liberen grandes cantidades de ATP. El ATP fuera de las células es microbicida, pero el tejido cardíaco activa mecanismos que degradan el ATP y lo transforman en adenosina, que tiene un potente efecto antiinflamatorio y desactiva la respuesta inmune, permitiendo la persistencia del parásito”, explicó Aoki.
Ante este fenómeno, el grupo de la FCQ demostró cómo todo este sistema resulta clave para detener la respuesta inmune, con el fin de evitar una inflamación exacerbada que protege al tejido cardíaco de las personas infectadas, pero a su vez favorece el desarrollo del parásito.
Basándose en este modelo, el equipo desarrolló otra línea para establecer los mecanismos por los cuales los pacientes diabéticos no responden tan eficientemente a las infecciones. Llamativamente, encontraron que el tejido cardíaco desarrolla potentes mecanismos de defensa contra el parásito, mientras que las defensas en circulación son muy deficientes.
Estos novedosos avances expusieron por primera vez el rol activo que desempeña el tejido cardíaco frente a una infección, así como en enfermedades metabólicas como la diabetes, lo que derivó en reconocimientos nacionales e internacionales para el equipo liderado por Aoki.
Según la investigadora, estos aportes han permitido identificar mediadores específicos de la respuesta cardíaca ante la infección por Trypanosoma cruzi, que permiten que este parásito permanezca en el tejido cardíaco durante décadas, y evidenciar mecanismos moleculares presentes en trastornos metabólicos como la diabetes, asociados a una menor respuesta de defensa.
“En cuanto a la optimización del tratamiento de la enfermedad con benznidazol, nuestro grupo propuso incrementar su eficacia disminuyendo la cantidad de droga administrada y adoptando esquemas más cortos, ya que la terapia actual es muy prolongada y está asociada a efectos colaterales por las altas dosis suministradas, lo que suele derivar en una alta tasa de abandono del tratamiento por parte de los pacientes”, explicó la científica.
De esta manera, el grupo realizó sustanciales aportes al conocimiento de la inexplorada inmunobiología del tejido cardíaco y propuso alternativas que mejorarían la terapéutica de la enfermedad de Chagas.
El rol clave de las células T regulatorias
El equipo dirigido por Eva Acosta también aborda la enfermedad de Chagas desde la inmunología, pero se enfoca en los mecanismos efectores de la respuesta inmune y de los procesos regulatorios durante la infección. En los últimos años, se centró en el análisis del papel que cumplen las células T regulatorias (Tregs).

“Buscamos comprender los mecanismos inmunológicos que determinan la evolución de la infección por Trypanosoma cruzi, y en particular cómo se regula el equilibrio entre el control de este parásito y el daño inflamatorio”, dijo la directora del equipo.
Y agregó: “Nuestro trabajo contribuye a entender por qué algunas personas desarrollan formas graves de la enfermedad, mientras que otras permanecen asintomáticas durante años. Comprender estos mecanismos es clave para explicar la evolución clínica de la infección. Se trata de investigación básica que, como punto de partida, resulta fundamental para pensar futuras estrategias terapéuticas más precisas”.
Estos estudios derivaron en otras investigaciones orientadas a identificar en qué medida este tipo de mecanismos son compartidos con otras enfermedades infecciosas, como el caso del COVID-19. “Actualmente, estamos comenzando a extender este enfoque al estudio del virus sincicial respiratorio”, anticipó Acosta.
Entre los avances del equipo, se destaca el valioso rol de las células T regulatorias, las cuales “no solo limitan la inflamación, sino que también activan programas asociados a la reparación tisular, lo que sugiere que cumplen un papel doble al controlar el daño y, además, favorecer la recuperación de los tejidos”, describió la inmunóloga.
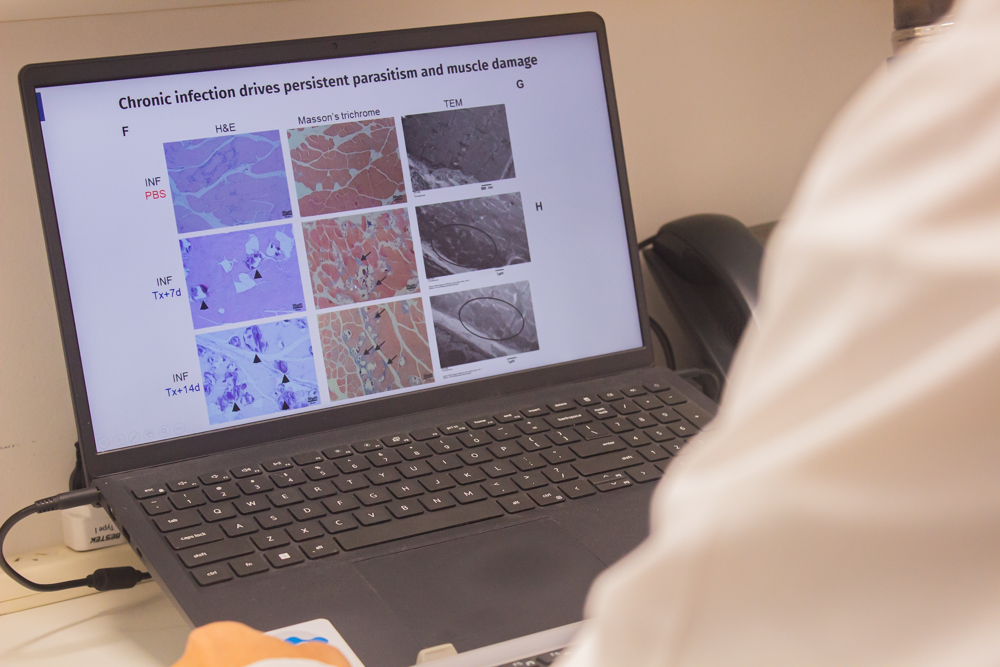
En base a esta perspectiva, las y los científicos de la FCQ también estudiaron qué sucede cuando se reducen estas células en el sitio de infección, demostrando que su presencia resulta clave para contener el daño, sin comprometer el control del parásito.
Los datos experimentales también comenzaron a vincular estos hallazgos con casos en humanos. Según Acosta, “los resultados abren la posibilidad de pensar en estrategias terapéuticas orientadas a promover o potenciar estas células, con el objetivo de prevenir el daño asociado a las formas más graves de la enfermedad y, al mismo tiempo, mejorar el control de la infección”.
En 2026, el grupo seguirá estudiando la caracterización de las células Tregs en este tema. A largo plazo, analizará enfoques de inmunoterapia que, si bien actualmente están desarrollados en el campo del cáncer y de enfermedades autoinmunes, sus aplicaciones en infecciones aún siguen siendo limitadas.
El compromiso de la Facultad de Ciencias Químicas (UNC) con la salud pública y la excelencia educativa sigue guiando el trabajo de sus diferentes equipos científicos, donde la expertise de sus docentes resulta clave para potenciar no sólo la calidad académica de las y los estudiantes formados en la universidad pública, sino también su rol activo ante problemáticas sociales como la enfermedad de Chagas.
Equipos
- Laboratorio de Biología Reproductiva e Inmunidad de Insectos. Directora: Lilián Canavoso. Integrantes: Leonardo Fruttero, Jimena Leyria y Pedro Paglione. Estudiantes: María Camila Dragonetti, Luis Berno, Estefanía Medici y Martina Rojas. Colaboradores: Fabián Ramos, Natalia Moyetta, Celia Carlini (Universidade Federal de Ciências da Saúde de Porto Alegre), Matheus Grahl Coste (Universidad Federal do Rio Grande do Sul) y Fernando Noriega (University of South Bohemia).
- Laboratorio de Inmunología Cardiovascular. Directora: María del Pilar Aoki. Integrantes: Gastón Bergero, Yanina Mazzocco, Sebastián Del Rosso. Estudiantes: Lara Gergolet, Azul Pons Demel, Camila Laspiur y Kenny Ryo Miyashiro. Colaboradores externos: Claudia Martínez Bernardi (Hospital Nuestra Señora de la Misericordia Nuevo Siglo), Laura Visconti (Hospital Nacional de Clínicas), Fernando Alfonso (Clínica Sucre), Carlos Quinteros Greco (Hospital Nacional de Clínicas) y Carlos Vigliano (Hospital Universitario Fundación Favaloro).
- Laboratorio del Departamento de Bioquímica Clínica y CIBICI. Directora: Eva Acosta Rodríguez. Integrantes: Luisina Onofrio, Camila Giménez, Florencia Bauer, Cristina Acosta y Daniela Porta. Colaboradores: Adriana Gruppi, Carolina Montes, María Carolina Amezcua e integrantes del Laboratorio GRUMA. Colaboradores externos: Ayelén González Montoya y Jorge Mukdsi.



